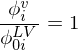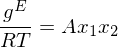Was ist UNIQUAC? Was ist UNIFAC?
UNIversal QUAsiChemical theory
Ist ein Aktivitätskoeffizienten Modell, das die Aktivitätskoeffizienten der Komponenten in einem chemischen Gemisch mit der Zusammensetzung, ausgedrückt durch Molenbrüche xi, korreliert.
Universal Function Aktivity Coeffizient
Analog zu UNIQUAC nur Moleküle in funktionelle Gruppen eingeteilt
Ist ein Aktivitätskoeffizienten Modell, das die Aktivitätskoeffizienten der Komponenten in einem chemischen Gemisch mit der Zusammensetzung, ausgedrückt durch Molenbrüche xi, korreliert.
Universal Function Aktivity Coeffizient
Analog zu UNIQUAC nur Moleküle in funktionelle Gruppen eingeteilt
Flashcard set info:
Author: CoboCards-User
Main topic: Thermodynamik
Topic: Thermodynamik 3
School / Univ.: TUHH
City: Hamburg
Published: 30.08.2011
Card tags:
All cards (31)
no tags



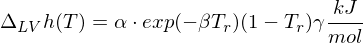



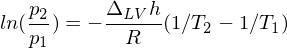
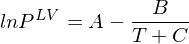



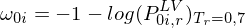


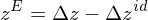


 ist Poyntingfaktor = 1
ist Poyntingfaktor = 1