Rule of Five?
1.) Molekülmasse ist nicht mehr als 500g/mol
2.) Das Molekül hat nicht mehr als 5 Donatoren (OH, NH, .... )
3.) Das Molekül hat nicht mehr als 10 Akzeptoren (O, N, ... )
4.) Verteilungskoeffizient zwischen Ocatanol/Wasser (log P) liegt zwischen -2 & 5
-> Trifft nicht immer zu: Taxol fällt heraus, ist jedoch hoch-wirksam!
2.) Das Molekül hat nicht mehr als 5 Donatoren (OH, NH, .... )
3.) Das Molekül hat nicht mehr als 10 Akzeptoren (O, N, ... )
4.) Verteilungskoeffizient zwischen Ocatanol/Wasser (log P) liegt zwischen -2 & 5
-> Trifft nicht immer zu: Taxol fällt heraus, ist jedoch hoch-wirksam!
Sauerstoffübertragungen
- Epoxidierung mithilfe einer Persäure
- Epoxidierung mithilfe von NBS
- Sharpless
- ....
- Epoxidierung mithilfe von NBS
- Sharpless
- ....
Tags: ToDo
Source:
Source:
Begriffsklärung: Arten von Isomeren?
- Konstitutionsisomere (gleiche Summenformel, andere Struktur)
=> sehr bekannt hier: Keto-Enol Tautomerie
- Stereoisomere
- Konformationsisomere (können durch Drehung an einer Bindung ineinander überführt werden)
- Konfigurationsisomere
=> Enantiomere/ Diastereomere
-
=> sehr bekannt hier: Keto-Enol Tautomerie
- Stereoisomere
- Konformationsisomere (können durch Drehung an einer Bindung ineinander überführt werden)
- Konfigurationsisomere
=> Enantiomere/ Diastereomere
-
Begriffsklärung: CIP-Regeln
- Zentralatom: 4 Substituenten a,b,c,d
- Molekül so anordnen, dass das niedrigeste von der OZ nach hinten steht (d)
=> im Uhrzeigersinn a->b->c->d => R
=> gegen Uhrzeigersinn a->b->c->d => S
Prioritätsregeln
1.) Ordnungszahl ( O > N > C > H )
2.) falls 1. Position identisch: Kette weiter folgen
3.) Doppel-/Dreifachbindungen: Betrachtung wie 2 bzw. 3 Bindungen.

- Molekül so anordnen, dass das niedrigeste von der OZ nach hinten steht (d)
=> im Uhrzeigersinn a->b->c->d => R
=> gegen Uhrzeigersinn a->b->c->d => S
Prioritätsregeln
1.) Ordnungszahl ( O > N > C > H )
2.) falls 1. Position identisch: Kette weiter folgen
3.) Doppel-/Dreifachbindungen: Betrachtung wie 2 bzw. 3 Bindungen.

Hantzsch - Widman Nomenklatur: Regeln
- Präfix wird in Reihenfolge der Tabelle vergeben
- bei gleichem Typ: "Di", "Tri"
- Nummerierung beginnt bei dem Heterogenatom, dass in der Tabelle am höchsten steht.
wenn bei Präfix und Suffix zwei Vokale aufeinander treffen, wird aus Gründen der Aussprache der Vokal aus dem Präfix entfernt.
Teilweise gesättigte Systeme:
- dihydro, tetrahydro, perhydro, ....
=> Tetrahydrofuran
=> 1,4-Dihydropyridin ( zwei Doppelbindungen von 2-3 & 4-5)
- bei gleichem Typ: "Di", "Tri"
- Nummerierung beginnt bei dem Heterogenatom, dass in der Tabelle am höchsten steht.
wenn bei Präfix und Suffix zwei Vokale aufeinander treffen, wird aus Gründen der Aussprache der Vokal aus dem Präfix entfernt.
Teilweise gesättigte Systeme:
- dihydro, tetrahydro, perhydro, ....
=> Tetrahydrofuran
=> 1,4-Dihydropyridin ( zwei Doppelbindungen von 2-3 & 4-5)
Flashcard set info:
Author: winnie
Main topic: Chemie
Topic: Organische Chemie
Published: 02.03.2010


























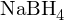 führt zu einem racemischen Gemisch!
führt zu einem racemischen Gemisch!
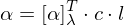

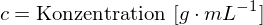


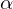






















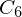 -
- ) sind sehr schwer
) sind sehr schwer - C_{...}##) sind schwer
- C_{...}##) sind schwer











